资讯详情
轮椅如何成功申请FDA510K
发布时间:2023-12-30 10:05:58
美国FDA定义电动轮椅是一种电池驱动的装置,其具有用于医疗目的的轮子,以便为限制坐姿的人提供移动性。
电动轮椅属于FDA II医疗器械,需要向FDA提交510K文件,并接受FDA技术审核。
手动轮椅,电动轮椅或电动代步车产品,进入美国市场需要申报510K。这类产品的申报比较复杂,企业在寻求咨询机构时,考察其是否具备同类产品申报成功经验很关键。
结合我司的在康复辅助器械510K申请中的成功案例,总结一下轮椅和代步车的美国市场准入要求如下:
1需要找到*合适的比对器械
轮椅和代步车种类繁多,型号也是各种各样,有电动或者手动折叠式,有两驱或者四驱式等等。
如何找到*合适的比对器械,从而缩短510K评审时间和提高评审通过率,这也是企业困惑*多和难以把握的地方。2需要有符合FDA格式&内容要求的检测报告众所周知FDA对于产品性能检测方面的检测机构没有太高的要求,但对于检测报告的内容和可读性要求较高。3需要有说服力的510K的技术文件电动轮椅和代步车产品零部件众多,还会涉及到风险评估,网络安全等方面。越是复杂的产品,FDA审核员会更为重视和仔细阅读,同时也会提出很多整改要求。
如果企业只是套用国内或CE注册的文件模板,对FDA的法规不够了解,英文水平有限,不能有效的回复FDA整改要求,都可能造成申请的失败。
电动代步车电动轮椅510K办理流程如下:
我们拥有独立的机械物理性能检测平台,可以提供按照ISO 7176系列标准检测的全项服务,且SUNGO出具的检测报告可以满足FDA评审要求,为客户提供咨询、注册和检测的一站式服务。
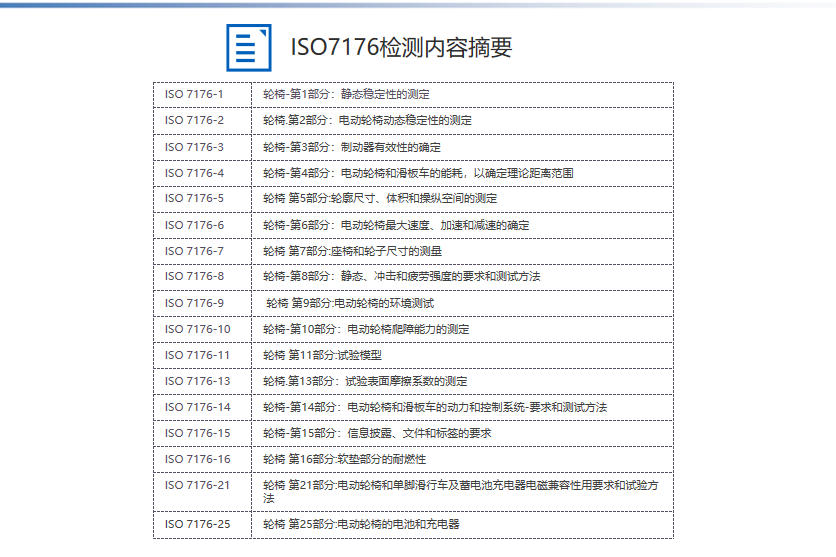
轮椅ISO7176检测标准:
SUNGO还可为电动轮椅/电动代步车客户开展检测服务,实验室配备全套**设备,符合欧盟和美国相关标准的要求,出具的检测报告已获得相关机构认可。
轮椅电动代步车510K批准信模板:

选择有配套检测的510K服务商可以节约企业对接成本以及检测报告更符合510K评审的要求。我们致力于国内康复产品轮椅走出国门走向欧盟美国,畅销海内外市场。
轮椅如何成功申请FDA 510K
在美国,所有产品制造商都需要通过FDA(美国食品药品监督管理局)的审核批准才能将产品投放市场。对于医疗器械,FDA要求制造商必须提交510(K)申请以获得市场批准。本文将为您介绍如何成功申请FDA510(K)批准,特别针对轮椅的申请。
申请流程
1.准备必要文件
首先,制造商需要确保轮椅产品符合FDA的标准。制造商需要在设计和生产过程中遵守美国法律规定,包括FDA相关标准。制造商需要收集以下文件
* 设计规格书 包含轮椅的所有设计规格,如尺寸、材料、功能等。
* 生产规格书 生产轮椅时使用的所有规范和流程。
* 验证/鉴定计划 用于验证轮椅符合FDA标准的方法。
* 临床数据 如研究、试验数据。
2.提交510(K)申请
申请人需要通过FDA的电子提交网站(https //www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfpmn/pmn_login.cfm)提交电子申请。其中包含以下信息
* 表格
* 设计规范和说明书
* 数据样本
* 支持文件
* 更多信息
3.评估和审核
一旦申请提交完成,FDA将对申请进行评估和审核。在审核过程中,FDA可能会要求制造商提交更多的文件或临床数据以查明产品的安全性和有效性。这个过程可能是*耗时的一部分,通常需要数月到数年的时间。
4.市场批准
如果申请部分或全部通过审核,FDA将颁发510(K)市场批准。制造商可以根据获得的批准开始销售轮椅。
对于轮椅的申请,申请人需要注意以下几个方面
1.轮椅分类
FDA根据等级制度对医疗设备进行分类。根据其风险性和预期用途,轮椅将被分为三类。一般情况下,FDA对等级高的轮椅的严格审查程度会更高。
2.利用临床数据
轮椅的申请需要提供临床数据以评估其有效性。制造商应该提供可用的研究和试验数据,并详细描述其轮椅的临床试验计划,进行系统性数据分析,确定它是否能在FDA标准下保持稳定的性能。
3.使用FDA标准
制造商需要使用FDA提供的验收标准,以确保产品符合FDA标准。制造商可以更新其制造和设计标准,适应FDA标准要求。
问答
1.申请510(K)需要多长时间
在FDA收到您的申请后,审核周期通常在3 6个月左右,甚至可能长达一年或更长时间,这取决于您的申请提交和FDA检查、验证及审定的次数。
2.什么是评估组
评估组由一组专家和FDA代表组成,对文件进行审核,同时进行临床数据的审核。
3.510(K)批准的有效期是多长时间
510(K)批准有效期是五年,但是申请人必须每五年更新申请。
结论
成功通过FDA的510(K)认证是制造商进入美国市场的必要步骤。申请人需要熟悉FDA的标准和程序,提交完整、高质量的申请,以确保个人或公司产品通过审批并获得上市批准。对于轮椅的申请,申请人应该特别注意对FDA标准的遵守和临床数据的有效使用,同时遵守FDA的规定和流程,确保申请的顺利通过。
资讯推荐
- 澳洲TGA注册澳代办理流程
- 出口澳大利亚的TGA注册:沙格在澳大利亚有自己的分公司:Sungo Australia Pty Ltd SUNGO可以提供:澳洲TGA技术文件编写,澳洲代表服务SPONSOR服务 以及完成澳洲TGA注册段落一:什么是澳洲TGA注册?澳洲TGA注册是指将医疗产品注册在澳大利亚治安和农村事务部(Therapeutic Goods Administration,简称TGA)的过程。TGA是负责监管和管理澳大利亚市场上的医疗产品和药品的机构,其使命是保护澳大利亚公众的健康和安全。通过TGA注册,产品可以在澳大利亚市场上合法销售和使用。段落二:澳代办理流程的必要性对于一些国际企业来说,直接进行TGA注}
- 2024-01-18 17:33:37
- 轮椅EN12183EN12184检测怎么做?
- 轮椅、代步车产品出口欧盟申请CE认证平均耗时2-3周,轮椅、代步车产品出口办理美国510K认证从项目申请到获批*快仅需58天!2021年至今美国FDA为中国大陆地区下发轮椅/代步车K号共40个,其中有16个产品K号是在沙格辅导下申请成功的,占总量接近50%。各类标准检测服务对于轮椅产品的检测,SUNGO提供按照GB/T 18029系列标准,ISO 7176系列标准和EN12183/EN12184标准进行检测的全项服务。第一段:介绍轮椅EN12183EN12184检测的重要性和意义。(约500字)在购买和使用轮椅时,进行EN12183EN12184检测是非常重要的。EN12183和EN1218}
- 2024-01-23 10:46:34
- 扩增仪提取仪荧光分析仪怎么办理欧盟IVDR CE
- 扩增仪提取仪荧光分析仪属于IVDR A类产品。CE合规路径和对应完成的工作是 :➢ 确定欧盟授权代表,签订欧盟授权代表协议➢ 在欧盟成员国主管当局完成注册登记(在荷兰药监局CIBG注册登记)➢ 依据MDR法规要求建立技术文件(含检测报告、GSPR、风险分析报告、临床评价报告、PMS计划)➢ 签署符合性声明(DOC)➢ 编制Basic UDI,注册SRN号,在EUDAMED数据库中完成注册第一段:欧盟IVDR CE认证是指根据欧盟2017/745号法规,在欧盟市场销售体外诊断医疗器械所必需的认证制度。扩增仪提取仪荧光分析仪作为一种体外诊断医疗器械,需要获得欧盟IVDR CE认证方可在欧洲市场}
- 2024-01-23 19:10:02
- 轮椅车的阻燃测试哪家可以做?
- 轮椅车属于医疗器械,因此轮椅车座靠垫的特性应符合使用者的医学需求,基于安全方面的考虑,轮椅车座垫不应该燃烧起火并释放出有毒气体伤害到其使用者和附近的人。目前具有阻燃性的轮椅车座垫,尤其是聚氨酯泡沫组件,可以通过添加或改变其化学组成成分使其达到阻燃安全的标准。但这一改进通常是以牺牲材料的舒适度、压力分布和耐用性等特征为代价的。因此,过高的阻燃性要求对实际使用中优质座靠垫的设计可能并无贡献,并阻碍有用的产品推向市场。图片事实上轮椅车着火并燃烧是很罕见的,美国1990年发布的期刊《美国与轮椅有关的致命事故》中收集的数据显示,每100万轮椅使用者中只有很小一部分人是死于火灾。美国FDA的公开记录表明}
- 2023-12-23 08:03:07
- 轮椅510K申请+检测一站式服务助力企业快速获得510K(K号)
- 近期,由SUNGO从产品测试到技术文件编写全程辅导的宁波某企业手动轮椅FDA 510K项目,从提交到获批仅历时2个月,便通过了FDA审核,产品可以合法合规的在美国市场自由流通!该企业的全套测试由沙格实验室开展,完全符合FDA的要求,覆盖到了FDA关切的所有点和面。再配合沙格咨询团队的综合实力和经验,使得项目进展十分顺利。全程无发补,60天获批。本次能够快速地通过FDA的严格评审,离不开SUNGO与企业的全力合作,同时,也无疑证明了双方在各自领域的可靠实力。沙格集团聚焦于检验检测服务的技术平台,经过了两年多的发展,目前已经建成了上海实验室、合肥实验室两个检测实验场地,实验室已获美国IAS认可}
- 2023-11-28 14:20:56
